トロスト先生の全合成 / Total synthesis report from B.M.Trost's lab.
はいこんにちわかほし〜
この間、セミナーでやった論文紹介するよー。
今回は、あのアリルケミストリーの第一人者、バリー・トロスト大先生の研究室から報告された、(–)-Perophoramidineの全合成についてお話しましょう。

Chem. Sci., 2014, Advanced Article. DOI : 10.1039/C4SC01826E
(+)-Perophoramidineは、2002年にIrelandらによってフィリピン産のホヤから単離構造決定*1され、2010年のQinらの不斉全合成によって、その絶対立体配置が決定されました*2。
構造の特徴としては、高度に官能基化された六環性骨格と二つのアミジン骨格、二つの連続する四級不斉中心が挙げられます。
今回紹介する論文は、天然物とは逆の旋光度を有する(–)-Perophoramidineをトロスト先生の研究室が開発した反応を使って合成してやろうと言った内容です。
大まかな合成計画は以下のようになってます。

本論文の注目ポイントは3つ!
- お家芸!モリブデン触媒による不斉アリル位アルキル化反応 (Mo-AAA) / Trost's speciality !! Molybdenum-catalyzed asymmetric allylic alkylation (Mo-AAA)
- アリル基を利用した巧みな化学変換 / Chemical transformation of allyl group
- 全体的に怪しい化合物の立体化学 / Questionable stereochemistry of the products through the whole
1. お家芸!モリブデン触媒による不斉アリル位アルキル化反応 (Mo-AAA) / Trost's speciality !! Molybdenum-catalyzed asymmetric allylic alkylation (Mo-AAA)
トロストらは、以前の研究で、3-アルキルオキシインドールを求核剤として用いるMo-AAAについて報告しており、モノ置換アリル化合物を求核剤として用いると、連続する3級、4級不斉中心をもつbranched型のアリルオキシインドールを高収率、高位置選択性、高立体選択性で得ることに成功しています*3。

この反応を使って、本化合物を合成する上で重要な、二つの不斉中心を構築出来たって言ってます。実際は後々、C-アリル化の際に一度立体がキャンセルされてしまうので、片方つくって、もう片方はジアステレオ選択的に構築ってところなんですけどね。
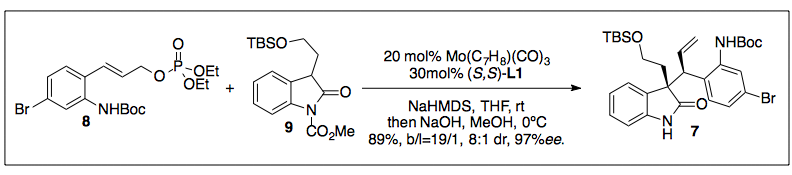

配位子はいわゆるトロスト配位子と呼ばれるタイプのモノ。いわゆる伝家の宝刀。
この反応は以下の錯体構造を経由して進行してるものと思われます。配位子のシクロヘキサン環とオキシインドール3位から伸びるアルキル鎖の障害の有無によってオキシインドールの面選択性が制御されてるんですね〜。たぶんですけど!

本反応は、どうやらクライゼン転位様に進行するという*4 らしいので、アリル位の立体については以下に示すようなイス型六員環遷移状態を経由しているものと考えました。

アリール基を比較的安定なエクアトリアル位に配置することでアリル位の立体が望みのそれとなります。
これが今回の鍵反応!
2. アリル基を利用した巧みな化学変換 / Chemical transformation of allyl group
合成上重要なビルディングブロックとなるアリル基。
アリルケミストリーの王様は、これをうまく使ってるぞ。
といっても常法っちゃ常法だけど…。
酸化開裂→酸化→エステル化→アミド化
酸化開裂→還元的アミノ化→縮合
とかね!Perophoramidineの上の二つの五、六員環は、両方ともアリル由来だぞ!
参考になりそ〜。
末端オレフィンてほんとうに便利で、そこを起点に酸化開裂とか、ヒドロホウ素化-酸化なんかして官能基変換がバンバンできちゃうってわけ!
3.全体的に怪しい化合物の立体化学 / Questionable stereochemistry of the products through the whole
これは正直どうなってるのかわからん。
どこかで絶対立体の確認をしてるわけでもなし、相対立体の確認をしてるわけでもなし…。そういったデータの記載がない。
まあ〜、過去の文献を見る限り、最初の立体構築はきちんと出来てるのかもしれないけどさ〜。
どこかで証拠を示してほしいってのが感想。ここのジャーナルはそういうこと言わんのかね?僕はセミナーで先生によく言われるよ。証拠を示せって!
僕が、全体的に怪しいッて思った最大の理由が、最終生成物の旋光度!つまり、天然物のエナンチオマーの旋光度!
天然物の旋光度 *1 [α]D (c 0.733, CHCl3) =+3.8
初めて不斉前合成された時の合成品の旋光度 *2 [α]D (c 0.5, CHCl3) =+3.9
今回合成されたエナンチオマーの旋光度 [α]D (c 1.10, CHCl3) = –26.4
なんか、怪しくない???
これってこれでいいの???
すごい疑問。エナンチオマーの旋光度ってエナンチオマーと絶対値は一緒になるんじゃないの??
まさかの天然物が混ざりのパターン???
それはないとは言い切れない。無いとは言い切れないけどさ。
納得できる説明、待ってます。
あ、あと25位メチル基のプロトンがmultipletになってる!天然物はちゃんとsingletだぞ!どうなってるんだ!!!!!!!!!!!!!!
今回はめんどいから英語なし!
それじゃあ!